La herramienta usada para esta minuciosa labor no ha sido una cámara, sino una técnica conocida como criomicroscopía electrónica que valió en 2017 el Premio Nobel de Química a Jacques Dubochet, Joachim Frank y Richard Henderson. Ellos sentaron las bases de este método, de cuya aplicación es pionera Nogales. "Comencé a trabajar con criomicroscopía a finales de los años 80, cuando aún estaba en su infancia", cuenta a XATAKA esta científica nacida en Madrid, que por entonces se encontraba en Reino Unido haciendo su doctorado. Ahora, Nogales dirige su propio laboratorio en la Universidad de California en Berkeley (EE.UU).
Durante todo este tiempo, la científica ha perfeccionado su abordaje de la técnica de la criomicroscopía electrónica, que ha empleado para estudiar muchos sistemas biológicos diferentes y conocer su estructura. "Entre ellos, los microtúbulos, que son una importante diana contra el cáncer", afirma Nogales. Es decir, una estructura a la que atacar para destruir las células cancerígenas. Ahora, Nogales protagoniza -junto con otras investigadoras asociadas también a Berkeley- un estudio de repercusión internacional publicado el miércoles en Nature.
Más allá de los límites
El foco del artículo son los telómeros: una repetición de secuencias de ADN que existe al final de cada cromosoma [estructuras que contienen la mayoría de la información genética de una persona] y lo protegen. Sin ellos -explica Nogales- las células pensarían que son cromosomas rotos que deben reparar y fusionaría unos con otros, "lo cual sería terrible". El problema es que cada vez que una célula se divide tiene que copiar el genoma - replicar el ADN- y, en este proceso, se van perdiendo trozos del final del cromosoma que no se copian. Esto provoca que los telómeros sean cada vez más cortos, hasta un punto en el que la célula se da cuenta de que algo no funciona y decide suicidarse o dejar de dividirse, lo que da lugar al envejecimiento.
El estudio de Nogales y sus colegas "proporciona una visión sin precedentes de cómo se organiza el complejo enzimático y establece un marco para el descubrimiento de fármacos", subraya Nature. Si bien se había ya conseguido alguna imagen de la estructura de la telomerasa, su resolución era muy pobre. En contraste, la lograda por las investigadoras de Berkeley es tres veces mejor, tomada a una escala por debajo de la nanométrica.
El problema era doble. Por una parte, la dificultad de aislar muchas copias de la telomerasa y conseguir aquellas que están activas. Por otra, la flexibilidad de la telomerasa, que dificulta conocer su estructura. Para sortear estas barreras, las investigadoras desarrollaron un procedimiento mejorado de purificación. "Necesitábamos dos cosas: mejorar la cantidad de telomerasa activa que éramos capaces de obtener y forzar los límites de lo que la criomicroscopía electrónica es capaz de hacer", explica. Y lo lograron.
De ahí la relevancia del estudio. "Los medios de comunicación no han parado de llamarnos en las últimas 24 horas", comenta. Y es que, en el ámbito científico, los telómeros son un tema candente por su relevancia para la biología celular, el envejecimiento humano, el desarrollo del cáncer, etc.. Y, hasta ahora nadie había sido capaz de obtener información sobre su estructura. "Este estudio ha traspasado muchos límites en lo que era técnicamente posible", afirma la española.
La investigación es también interesante por otros motivos, más allá de los telómeros. Nogales señala que, gracias a esta, se conoce un proceso no descrito nunca antes, que es extrapolable a otros sistemas biológicos y que es crítico, por ejemplo, en la regulación de la expresión génica o epigenética [lo que determina qué genes se expresan y cuáles no, y con ellos la capacidad humana para adaptarse al medio].
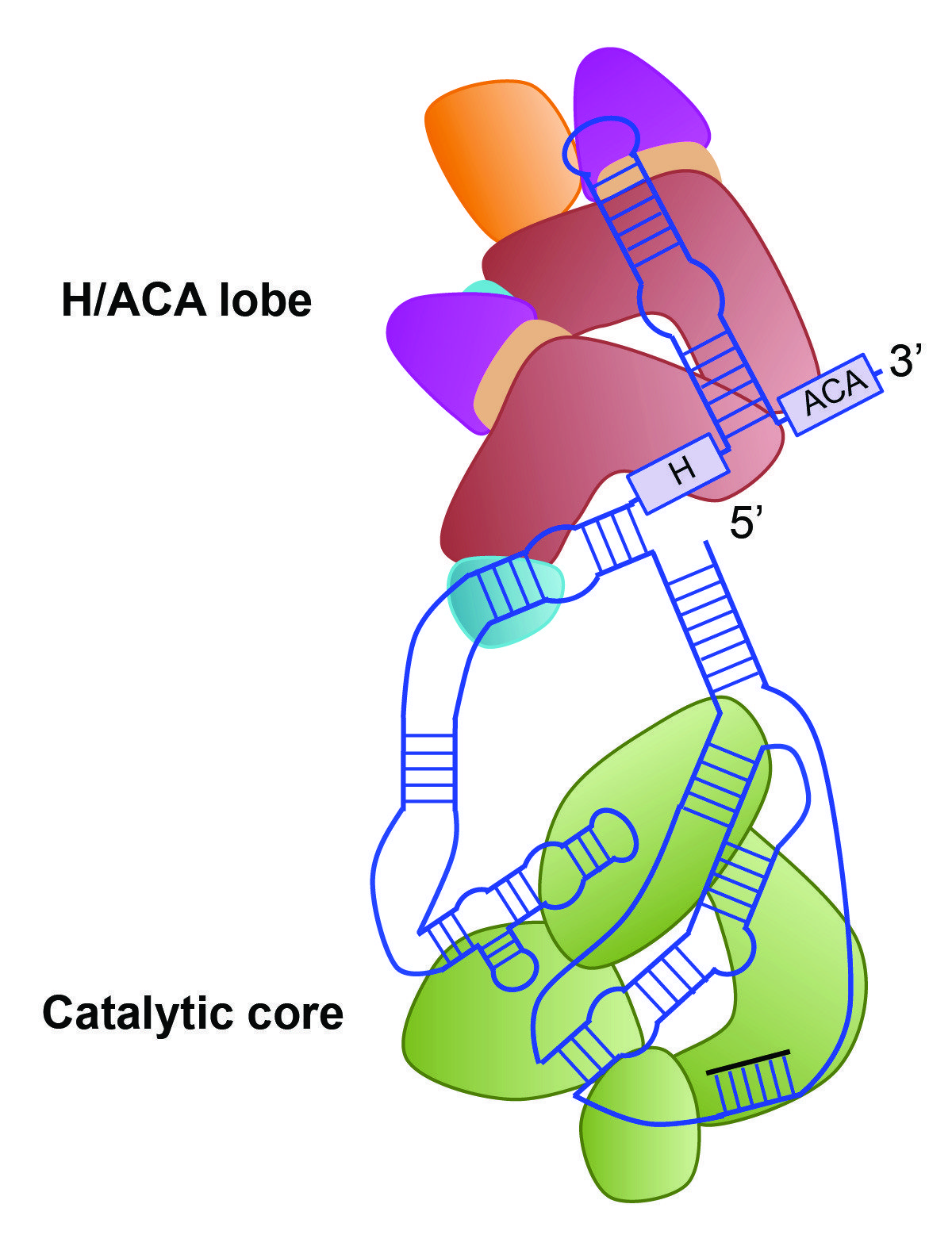
Dibujo de la la telomerasa humana cedido por Eva Nogales. Su estructura general es bilobal (con dos lóbulos) y consiste en un ARN extendido que actúa como andamio para varias proteínas. El lóbulo H/ACA facilita el ensamblaje de la telomerasa a partir de sus componentes y controla el tráfico en el núcleo. El otro lóbulo contiene el núcleo catalítico de la enzima.En qué se traduce esto
Una de las primeras cosas que se puede hacer una vez conocemos esas estructuras -explica Nogales- es mapear las mutaciones genéticas que fomentan el desarrollo de diferentes enfermedades dentro de la estructura de la telomerasa, lo que proporciona un mejor conocimiento de la razón por la cual esa mutación causa dicha enfermedad. "Esto es crítico para pensar sobre cómo tratar a los pacientes afectados", afirma.
El desarrollo de medicamentos dirigidos a un punto específico de la célula es otra aplicación fundamental de este hallazgo. "Conocer la estructura de la telomerasa como actor fundamental en la salud humana es un primer paso para el diseño de este tipo de fármacos", asegura la científica. Los usos posibles de estas medicinas son múltiples, empezando por el cáncer, ya que con ellas se evitaría la destrucción de células sanas que ocurre con los quimioterápicos actuales.
Por otra parte, son también interesantes tratamientos anticáncer contra la telomerasa. Como explica Nogales, esta enzima es la que hace que las células cancerígenas sean inmortales. Por ese motivo, la española señala que hay que ser precavidos en el la estrategia antienvejecimiento basada en telómeros, ya que tratar de convertir en inmortales en todas las células puede ser un arma de doble filo. "El cáncer no deja de ser una célula inmortal que ha perdido su identidad y se reproduce de forma descontrolada. Si la telomerasa fuera siempre funcional, podría facilitar su desarrollo. De alguna manera, hacer que los telómeros se acorten es una forma de mantener el medio seguro para tratar de impedirlo", explica.
La investigadora Mariana Castells, catedrática de la Escuela Médica de Harvard, señala otro ámbito de utilidad del estudio publicado en Nature: la clonación. El desconocimiento de la telomerasa -afirma Castells- fue uno de los motivos de la muerte temprana de la oveja Dolly. "En procesos de clonación hay que asegurarse de que los telómeros son funcionales, que están en buen estado", afirma Nogales, que reconoce no ser experta en este campo.
Ciencia multidisciplinar, y en femenino
Tampoco la telomerasa es el fuerte de Nogales, por eso se alió con otras científicas procedentes de diversos campos. "Este es un trabajo que no se podría haber hecho solo en el laboratorio de Katty Collins o en el mío", afirma. En su opinión, es una muestra de lo importante que la multidisciplinariedad en la investigación entre campos que son complementarios y que un laboratorio de forma aislada no puede realizar. Es un trabajo de años, que implica la colaboración de expertos en diferentes campos.
Nogales también destaca que las dos directoras de laboratorio y la investigadora joven que realizo la mayoría del trabajo (Kelly Nguyen) son todas mujeres. "No nos asusta el riesgo. Vemos algo importante y vamos a por ello, cueste lo que cueste", asegura. Esto -sostiene- da una idea de hacia dónde va la investigación: hacia la colaboración y hacia el liderazgo femenino en la 'ciencia de riesgo'. "Las mujeres cada vez tenemos un papel más relevante en ciencia que es puntera, en la que las posibilidades de que algo no salga bien son muy grandes pero que, de hacerlo, tiene mucho impacto", sentencia.
Y, ya que hablamos de científicas pioneras y telomerasa, no podíamos dejar de mencionar a la española María Blasco, directora del Centro Nacional de Investigaciones Oncológicas (CNIO). En 2008, su grupo de investigación en el CNIO fue uno de los primeros en descubrir unos componentes teloméricos llamados Terra. Desde entonces, se han propuesto descifrar su función. Recientemente han dado importante paso en ello. Como muestra un estudio publicado este mismo mes en Nature Communications, los Terra juegan un papel decisivo en el ensamblaje de la heterocromatina telomérica. Es decir, que son importantes reguladores epigenéticos.




Comentarios del Lector
a nuestro Boletín