Unos científicos que estudian una bacteria primaria de las responsables de la tuberculosis y la lepra han descubierto una enzima que convierte el hidrógeno en electricidad, y creen que podría utilizarse para crear una nueva fuente de energía limpia literalmente del aire.
Ahora, al extraer y estudiar la enzima, los investigadores afirman haber encontrado una nueva fuente de energía que podría utilizarse para alimentar una serie de pequeños dispositivos eléctricos portátiles. Sus hallazgos se publican el 8 de marzo en la revista Nature.
"Nos imaginamos que una fuente de energía que contenga Huc podría alimentar una serie de pequeños dispositivos portátiles que utilizan aire, incluyendo sensores biométricos, monitores ambientales, relojes digitales y calculadoras u ordenadores sencillos", dijo a Live Science por correo electrónico el autor principal Rhys Grinter, microbiólogo de la Universidad de Monash en Australia.
"Cuando proporcionas a Huc hidrógeno más concentrado produce más corriente eléctrica", explicó. "Lo que significa que podrías utilizarlo en pilas de combustible para alimentar dispositivos más complejos, como relojes inteligentes, o smartphones, ordenadores portátiles más complejos, y posiblemente incluso un coche".
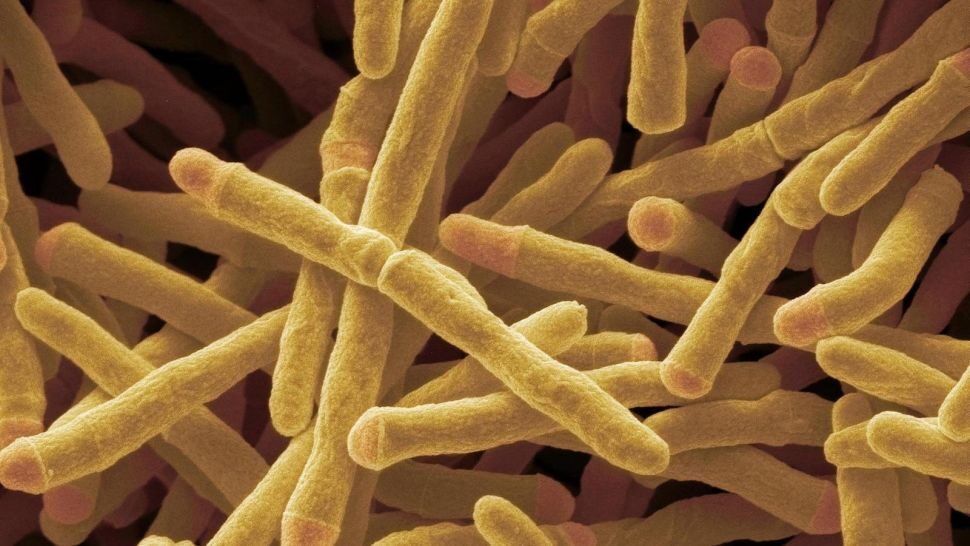
La M. smegmatis es una bacteria no patógena de crecimiento rápido que suele utilizarse en el laboratorio para estudiar la estructura de la pared celular de su pariente cercano, Mycobacterium tuberculosis. Se sabe desde hace tiempo que la M. smegmatis, presente en el suelo de todo el mundo, convierte en energía las trazas de hidrógeno presentes en el aire; de este modo, el microbio puede sobrevivir en los entornos más difíciles, como los suelos antárticos, los cráteres volcánicos y las profundidades oceánicas, donde apenas puede encontrar otro combustible, explican los investigadores.
Pero hasta ahora, cómo lo hacía la M. smegmatis era un misterio.
Para investigar la química que subyace a la sorprendente capacidad de la M. smegmatis, los científicos aislaron primero la enzima Huc responsable del proceso mediante cromatografía, una técnica de laboratorio que permite a los científicos separar los componentes de una mezcla. A continuación, investigaron la estructura atómica de la enzima con criomicroscopía electrónica, una técnica que valió a sus creadores el Premio Nobel de Química de 2017. Al proyectar electrones sobre una muestra congelada de Huc obtenida de M. smegmatis, los investigadores cartografiaron la estructura atómica de la enzima y las vías eléctricas que utiliza para transportar los electrones de modo que formen una corriente.
El equipo descubrió que, en su centro, Huc tiene una estructura, denominada sitio activo, que contiene iones cargados de níquel y hierro. Una vez que las moléculas de hidrógeno (formadas por dos protones y dos electrones) entran en el sitio activo, quedan atrapadas entre los iones de níquel y hierro y son despojadas de sus electrones. A continuación, la enzima envía estos electrones en un flujo que genera una corriente.
"Los electrones son absorbidos por Huc (concretamente por el ion de níquel) y transferidos a la superficie de Huc (mediante un hilo molecular formado por grupos de iones de hierro y azufre)", explica Grinter. "Si inmovilizamos Huc en un electrodo, los electrones pueden entrar en un circuito eléctrico desde la superficie de la enzima y generar corriente".
Otros experimentos revelaron que la enzima Huc aislada puede almacenarse durante periodos prolongados; que sobrevive congelada o calentada hasta 80 grados Celsius (176 grados Fahrenheit); y que puede consumir hidrógeno en concentraciones tan minúsculas como el 0,00005% del que se encuentra en el aire que respiramos. Según los investigadores, estos atributos, junto con la ubicuidad del microbio y su facilidad de cultivo, podrían hacer de la enzima una candidata ideal como fuente de energía para baterías orgánicas.
"Huc puede extraer energía del hidrógeno del aire, que es ilimitado", afirma Grinter. "La cantidad de electricidad que puede generarse a partir de las bajas concentraciones de hidrógeno en el aire será modesta. Esto limitará la aplicación de Huc en este contexto a dispositivos que requieran una cantidad pequeña pero sostenida de energía". Un uso complementario de Huc sería en pilas de combustible donde se proporciona una mayor concentración de hidrógeno".
Ben Turner es redactor de Live Science en Reino Unido. Se ocupa de física y astronomía, entre otros temas como la tecnología y el cambio climático. Se licenció en Física de Partículas en el University College de Londres antes de formarse como periodista.



Comentarios del Lector
a nuestro Boletín