Desde que empecé mis estudios de medicina, he leído todo lo que he podido leer sobre mi profesión, pero también sobre temas relacionados. Todavía lo hago, aunque sólo sea porque me gusta mucho leer, y hasta hoy no he terminado de aprender y leer. A lo largo del camino, para mi sorpresa al principio, he aprendido que muchos de mis colegas no lo hacen, y se limitan a la formación obligatoria y (a veces) a las directrices. Hay varias razones para ello que no mencionaré aquí.
Sin embargo, también es difícil mantenerse al día con la literatura médica, dado el gran número de artículos que aparecen a diario. Es una tarea considerable separar el trigo de la paja de esta literatura médica. La lectura de los informes de investigación científica propiamente dicha (comparada con la lectura de revisiones e informes de casos) es una tarea bastante grande, ya que requiere mucho tiempo y esfuerzo para formarse al menos una valoración general de la metodología y las estadísticas utilizadas, y poder evaluar si la investigación se ha llevado a cabo correctamente.
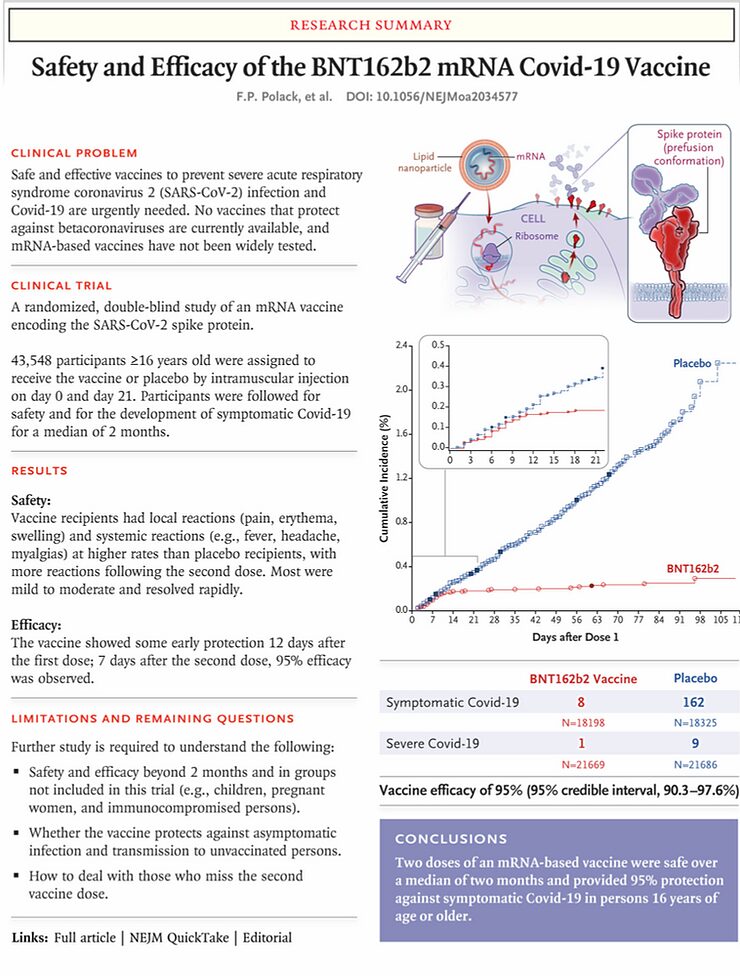
Y sin embargo, eso es lo que intentaré hacer aquí, de nuevo. Se trata, por supuesto, de los datos sobre la vacuna de Pfizer/BioNTech contra el virus del SARS-CoV-2, que se publicaron en línea el 10 de diciembre en la página web del New England Journal of Medicine.
"Seguridad y eficacia de la vacuna BNT162b2 mRNA Covid-19".
https://www.nejm.org/doi/full/10.1056/NEJMoa2034577?query=featured_home
Esta vacuna de Pfizer/BioNTech contra el virus del SARS-CoV-2 fue aprobada por la Agencia Europea del Medicamento el lunes 21 de diciembre de 2020, y será la primera vacuna utilizada en los Países Bajos contra este virus. Se espera mucho de ella, aunque hasta esta publicación sólo se disponía de los comunicados de prensa del propio fabricante, que generalmente no es la fuente más fiable de información científica.
Es bueno enumerar con calma todos los hechos y datos, para ver lo que se sabe de esta vacuna, pero sobre todo para ver también lo que aún no se sabe. Empezaré por el resumen del artículo porque ya plantea más preguntas que respuestas.
"BNT162b2 es una vacuna de ARN modificado con nucleósidos, formulada con nanopartículas lipídicas, que codifica una proteína de pico de longitud completa del SARS-CoV-2 anclada en la membrana y estabilizada por prefusión"
Esta es la vacuna de la que estamos hablando. Se basa en un ARN mensajero (ARNm) que se estabiliza cambiando algunos de los nucleósidos (los componentes básicos del ARN) para que el cuerpo no descomponga el ARNm con demasiada rapidez. Este ARNm codifica la proteína pico del virus del SARS-CoV-2, la parte más inmunógena del virus. Esta proteína de espiga es la que permite al virus entrar en una célula al unirse al receptor ACE2. Posteriormente, este ARNm se introduce en las células (musculares) a través de pequeñas partículas, que entonces expresan el ARNm, y la "proteína pico" del virus se coloca en su propia membrana celular, de la misma manera que está en la membrana del virus. Allí es reconocida por las células del sistema inmunitario y así se desencadena la respuesta inmunitaria. Esta técnica de vacunación es nueva y nunca se había utilizado antes.
Comentario: Vea también (en inglés):
- A medida que la vacuna Covid-19 de Moderna toma la delantera, la promoción de su Jefe Médico de las "vacunas editoras de genes" sale a la luz
- "Se le miente a los sujetos a un grado criminal": Lo que no se dice acerca de la nueva vacuna contra el Coronavirus de Pfizer"
- ¡Vacunas del futuro de ADN y ARNm!
La sección de "Conclusiones" del resumen del artículo dice así: "Un régimen de dos dosis de BNT162b2 confirió un 95% de protección contra el Covid-19 en personas de 16 años o más. La seguridad durante una media de 2 meses fue similar a la de otras vacunas víricas". Esto significa que simplemente no sabemos nada acerca de la seguridad de esta vacuna durante un período de más de dos meses. Esos datos simplemente no están disponibles.
Pero eso no es todo. En la introducción del artículo se afirma que la recopilación de datos de los estudios de fase 2/3 que se ocupan de la "inmunogenicidad" y la "durabilidad" de la respuesta inmunitaria -el grado en que la vacuna es capaz de provocar una respuesta inmunitaria y la duración de esta respuesta inmunitaria- todavía está en curso y no se informa de ello en el artículo. En términos generales, esto significa que no se sabe si la vacuna es capaz de inducir una respuesta inmunitaria permanente, que protegería permanentemente al receptor contra la infección por el virus del SARS-CoV-2.
¿A quién no se le permitió participar en el estudio?
En cualquier estudio que analice el efecto de un medicamento o una vacuna, es importante saber a quién se le permitió participar en el estudio, y especialmente a quién no. Esto es importante para la validez interna de la investigación, pero sobre todo para la validez externa. La "validez interna" es un término que describe el grado de eficacia del fármaco o la vacuna para las personas que no participaron en el estudio, pero que se corresponden con las características de los participantes en el estudio. En general, se puede suponer que es así.
Sin embargo, es más importante el concepto de "validez externa": La cuestión de si los resultados del estudio se aplican también a personas cuyas características no se corresponden con las de los participantes en el estudio. En otras palabras, ¿se puede considerar que el fármaco o la vacuna funcionan igual de bien en personas con características distintas a las de los participantes en el estudio? Esa es siempre la pregunta que hay que responder antes de aplicar en la práctica los resultados de la investigación científica. En resumen: ¿los resultados de esta investigación científica se aplican al paciente que está sentado frente a mí en la consulta? A menudo no es así.
https://www.thelancet.com/journals/lancet/article/PIIS0140-6736(04)17670-8/fulltext
Por lo tanto, es muy importante en este estudio observar a las personas que no pudieron participar en el mismo. Los principales criterios de exclusión para este estudio fueron "antecedentes médicos de Covid-19", "tratamiento inmunosupresor" o "diagnóstico de una enfermedad inmunodepresiva".
Tenga en cuenta que estas son probablemente las personas que más temen infectarse con el virus del SARS-CoV-2 y que quieren vacunarse. Por lo tanto, este enfoque ha sido criticado desde varios puntos de vista porque los "criterios de exclusión" estaban definidos de forma muy amplia, y los investigadores tenían un gran grado de libertad en cuanto a quién incluían y a quién no en el estudio. Ahora se puede asumir que el riesgo de enfermedad grave y muerte como resultado de una infección por el virus del SARS-CoV-2 aumenta con la edad, y también es considerablemente mayor en personas con múltiples enfermedades subyacentes, lo que se resume con el término "comorbilidad".
Los investigadores que condujeron este estudio:
Lo siguiente que debemos preguntarnos es: ¿quién diseñó, realizó, analizó y publicó el estudio? La respuesta es bastante clara: el fabricante. Se trata de un estudio diseñado, realizado, analizado, publicado y pagado por la propia Pfizer/BioNTech. El hecho de que un comité independiente de datos y seguridad haya podido ver los datos no cambia esto, simplemente porque no tuvieron voz en el diseño de la investigación, la selección de los participantes, las estadísticas utilizadas o la publicación.
No hace falta que explique aquí cómo una construcción de este tipo puede llevar a resultados sesgados de la investigación científica, porque se ha investigado y publicado ampliamente sobre ello en los últimos veinte años.
https://jamanetwork.com/journals/jama/article-abstract/196846
John Ioannidis, en su monumental publicación "Why Most Published Research Findings Are False" (Por qué la mayoría de los resultados de investigación publicados son falsos) en la revista PLoS en 2006, señaló una vez más en el "Corolario 5":
"Cuanto mayores sean los intereses y prejuicios financieros y de otro tipo en un campo científico, menos probable será que los resultados de la investigación sean verdaderos".
https://journals.plos.org/plosmedicine/article?id=10.1371/journal.pmed.0020124
Comentario: Para mayor información sobre John Ioannidis, vea (en inglés):
- El epidemiólogo John Ioannidis sobre el fiasco del COVID-19: "Estamos tomando decisiones sin datos confiables"
- Los creadores de modelos estaban "astronómicamente equivocados" en sus predicciones subre el COVID-19, dice el epidemiólogo Dr John Ioannidis - y el mundo está pagando el precio
- Epidemiólogo Dr John Ioannidis de la Universidad de Stanford acusa a los medios de ocasionar pánico en el público por el Covid-19
Los puntos finales primarios y secundarios del estudio:
Los "criterios de valoración" primarios y secundarios en un estudio médico son un síntoma o conjunto de síntomas que se utilizan para determinar si el fármaco que se está probando es eficaz o no. En el caso de un fármaco diseñado para prevenir los infartos, por ejemplo, un "criterio de valoración primario" podría ser el dolor de pecho. Si alguno de los participantes en el ensayo desarrolla dolor torácico durante el mismo, alcanza el "punto final" y es retirado del ensayo. Estos datos sobre el número de personas que desarrollaron dolor torácico (no como resultado del ensayo, sino a pesar de él) y los que no lo hicieron se utilizarían para determinar la eficacia y seguridad del fármaco.
El "punto final" principal del estudio sobre la vacuna de Pfizer se define de la siguiente manera:
"La aparición de COVID-19, mediante la confirmación de un resultado positivo en la RT-PCR".
No voy a discutir la falta de fiabilidad de las pruebas RT-PCR en el diagnóstico de COVID-19 aquí, ya que ha sido ampliamente discutido y puede ser considerado como conocimiento común. Ya lo describí ampliamente en mi anterior entrada del blog, el pobre rendimiento de esta prueba en la práctica clínica ha sido ahora descrito en varios estudios científicos bien realizados.
https://www.janbhommel.com/post/de-verduistering
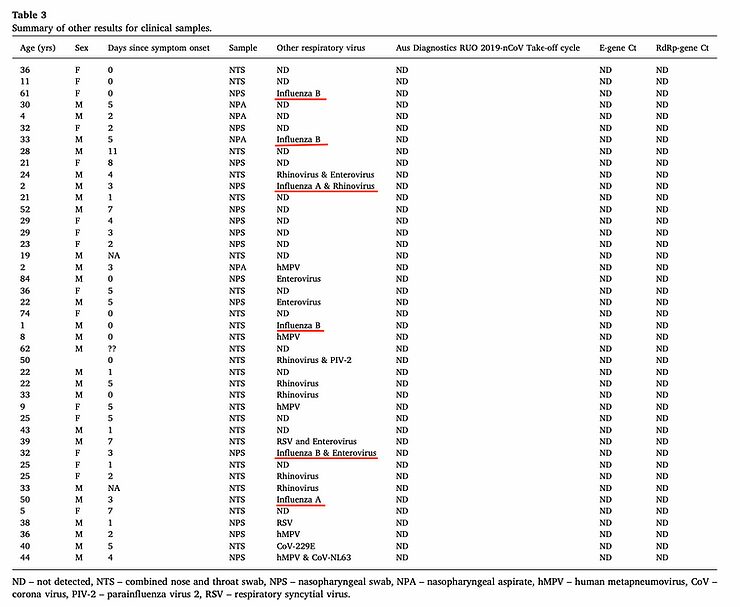
Más importante es la forma en que definieron la COVID-19. La definición es la siguiente:
"La COVID-19 confirmada se definió según los criterios de la Food and Drug Administration (FDA, Administración de Comida y Drogas) como la presencia de al menos uno de los siguientes síntomas: fiebre, tos nueva o aumentada, dificultad respiratoria nueva o aumentada, escalofríos, dolor muscular nuevo o aumentado, pérdida nueva del gusto o del olfato, dolor de garganta, diarrea o vómitos, combinados con una muestra respiratoria [es decir, un resultado positivo de la RT-PCR] obtenida durante el periodo sintomático o en los 4 días anteriores o posteriores"Tenga en cuenta que uno de estos síntomas en combinación con un resultado positivo de la RT-PCR para el virus del SARS-CoV-2 fue suficiente para diagnosticar el COVID-19. Un síntoma fue suficiente. El estudio no indica cuántos síntomas tenían las personas con COVID-19 ni la gravedad de estos signos o síntomas. Este estudio tampoco buscó otros agentes (virales) de estas dolencias y síntomas, mientras que al menos un estudio sugiere que cuando se sospecha de COVID-19 a menudo hay otros agentes (virales) que podrían explicar las dolencias y los síntomas. En ese estudio de 50 personas, 5 personas tuvieron finalmente un resultado positivo en la RT-PCR para el virus SARS-CoV-2, pero 6 personas tuvieron un resultado positivo en la RT-PCR para la gripe A o B.
https://www.sciencedirect.com/science/article/abs/pii/S1386653220301165
En cuanto a la definición de COVID-19 en el estudio, no hace falta decir que se trata, sin excepción, de síntomas para los que el médico de cabecera aconsejaría tomar un paracetamol y meterse en la cama. Sin excepción, son síntomas para los que la gente generalmente ni siquiera consulta al médico. Por lo tanto, es muy cuestionable la relevancia del diagnóstico de COVID-19 si se define de esta manera.
Sin embargo, también había una medida de resultado secundaria y es la aparición de "COVID-19 grave". Aquí tampoco es necesario explicar que la única medida de resultado que importa es: ¿hasta qué punto una vacuna contra el virus del SARS-CoV-2 es capaz de mantener a la gente fuera del hospital, hasta qué punto la vacuna es capaz de evitar el ingreso en cuidados intensivos y hasta qué punto la vacuna es capaz de evitar que la gente muera por la infección? Esas son las medidas de resultado más importantes, de eso se trata. Volveré a hablar de ello más adelante.
¿A quiénes sí se les permitió participar en el estudio?
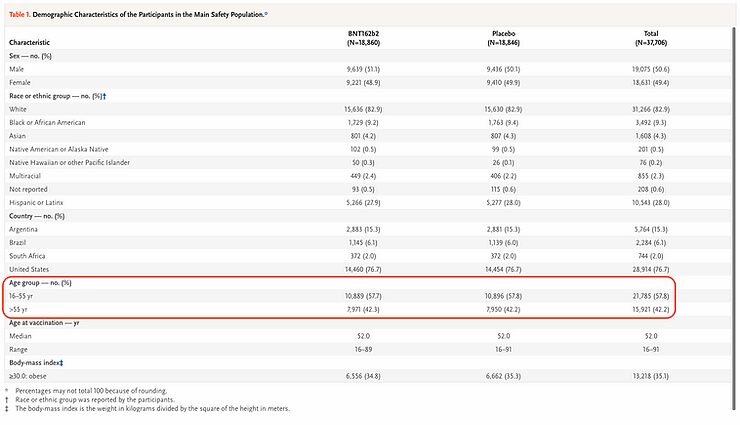
El siguiente paso es, por supuesto, examinar los rasgos y características de las personas que se incluyeron en el estudio. En primer lugar, la edad de los participantes. Casi el 58% de los participantes en este estudio sobre la vacuna contra el SARS-CoV-2 tenían entre 16 y 55 años. Es este grupo de edad, casi 2/3 de los participantes en este estudio, el que tiene poco que temer por la infección con el virus del SARS-CoV-2, y por lo tanto una vacuna tiene poco valor para ellos. Incluso cabe preguntarse, con lo que ahora se sabe sobre la tasa de mortalidad por infección del virus del SRAS-CoV-2, desglosada por edades, si es ético incluir a estas personas en el estudio. También volveré a hablar de ello más adelante.
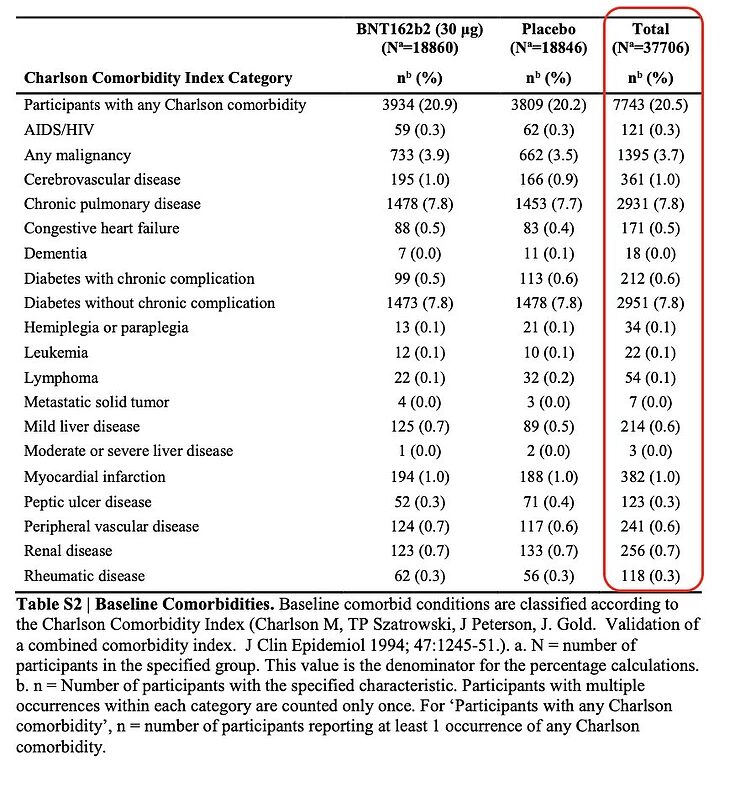
Esto también es evidente por las condiciones subyacentes (comorbilidad) de los participantes en el estudio. En total, sólo una de cada cinco personas parece tener una afección subyacente, y en el caso de las distintas afecciones subyacentes individuales, el porcentaje de personas que las padecen suele ser inferior al 1%.
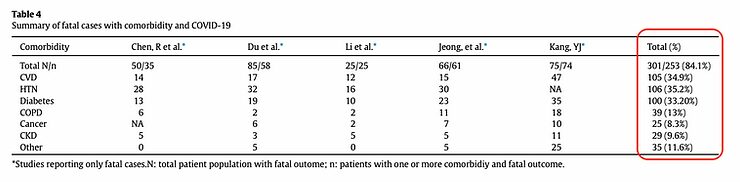
Qué diferencia hay entre las personas que enferman gravemente y mueren a causa de la COVID-19. La tabla siguiente procede de un estudio sobre la comorbilidad en los casos mortales de COVID-19. La tabla muestra que 9 de cada 10 personas tienen una condición subyacente que aumenta el riesgo de un curso grave de COVID-19.
https://www.ajicjournal.org/article/S0196-6553(20)30637-4/pdf
Si se vacuna a personas en residencias de ancianos y a personas mayores, el porcentaje de personas con una enfermedad subyacente será muchas veces mayor que entre los participantes en el estudio sobre la vacuna de Pfizer/BioNTech. Me temo que la comorbilidad en este grupo de personas es más bien del 80% en lugar del 20%, y tal vez incluso más. Por lo tanto, la validez externa de este estudio para las personas que viven en residencias de ancianos y las personas mayores es muy limitada, porque son precisamente estas personas las que no participaron en el estudio. Y son precisamente estas personas las que temen una infección por el SARS-CoV-2 y las que más tienen que ganar con una vacuna eficaz y segura.
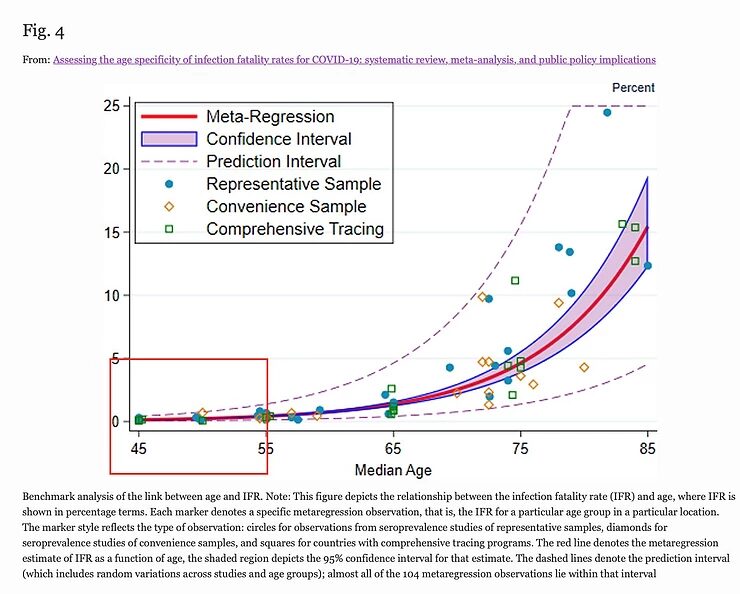
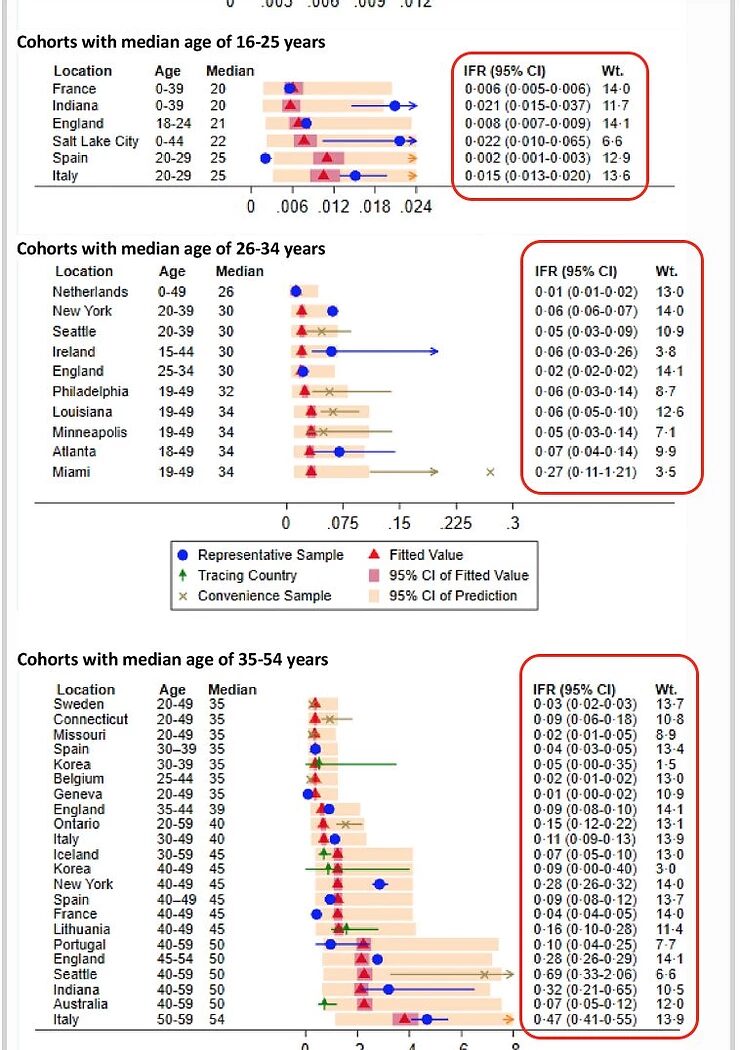
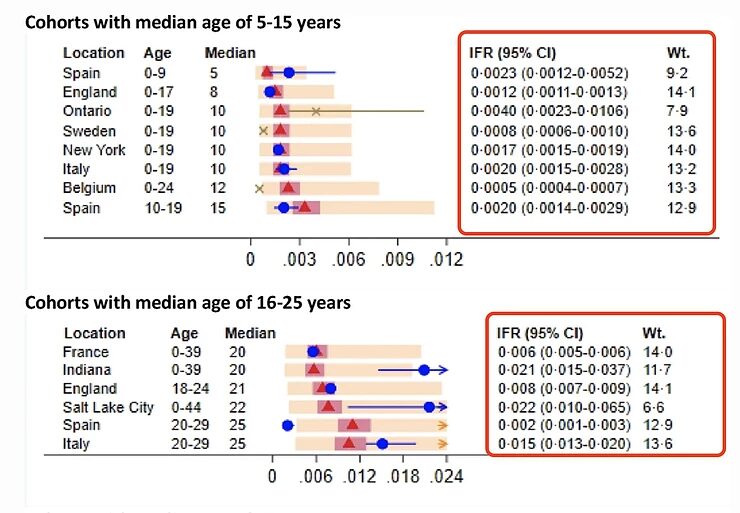
Hace muy poco se publicó un artículo sobre la tasa de mortalidad por infección (TMI) del virus del SRAS-CoV-2 en función de la edad. En él se desglosa la TMI de una infección por el virus SARS-CoV-2 en diferentes grupos de edad. Este tipo de investigación tiene sus trampas y escollos, pero es el mejor dato disponible que tenemos actualmente.
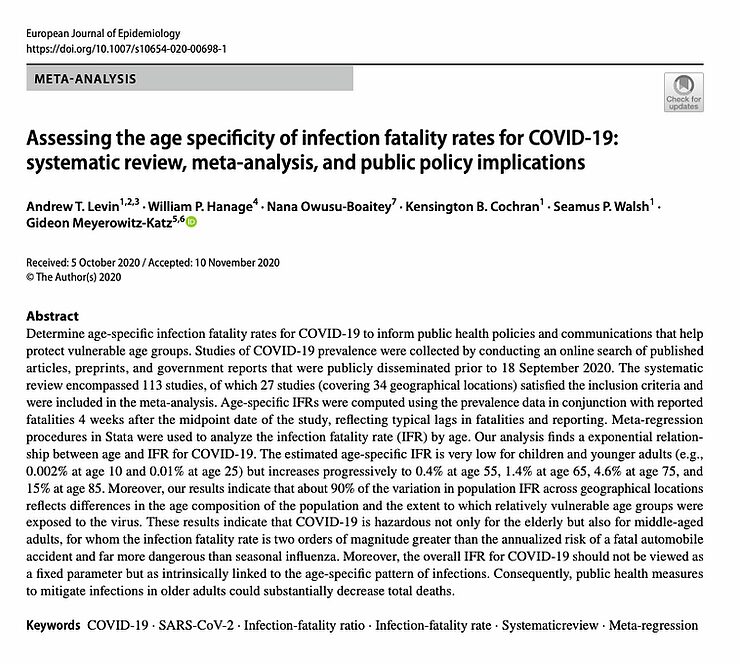
Utilizaré dos gráficos de este estudio que ilustran mi afirmación de que el grupo de edad entre 16 y 55 años tiene muy poco que temer del virus SARS-CoV-2: la estimación más alta de la TMI en el grupo de edad de 35 a 54 años es del 0,4%, pero la mayoría de las estimaciones están entre el 0,1 y el 0,2%. En los grupos de edad más jóvenes, la TMI es mucho menor, y en el caso de los niños es incluso más baja que en el caso de la gripe.
Cada año, en Estados Unidos, mueren entre 100 y 150 niños a causa de la gripe, una cifra enorme en comparación con las muertes de un solo dígito por el virus SARS-CoV-2 entre los niños. Incluso una infección por el virus respiratorio sincitial (virus RS) causa muchas más muertes entre los niños que el virus SARS-CoV-2. https://lci.rivm.nl/richtlijnen/rsv-infectie
Esto significa que, en este grupo de edad, entre 1 y 2 personas de cada 1.000 morirían a causa de una infección por el virus del SRAS-CoV-2, siendo las personas con enfermedades subyacentes las que corren mayor riesgo. Una vacuna debe ser ya muy eficaz y segura si quiere mejorar el pronóstico de estas personas.
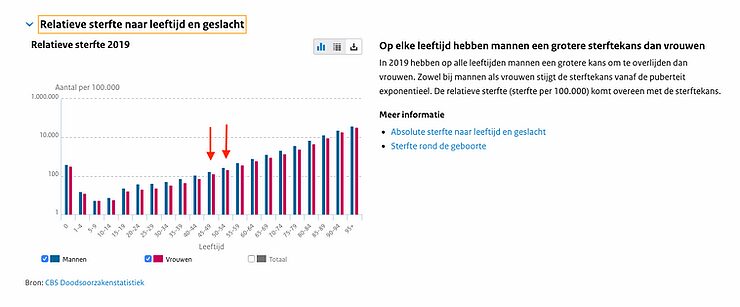
Además, si se observa la mortalidad específica por edad de una persona de 45 años, esta también es de 1 entre 1000, y por tanto no se desvía mucho de la mortalidad estadísticamente esperada a esta edad. No se puede decir simplemente que esto duplica el riesgo de muerte, porque la gente sólo puede morir una vez.
https://www.volksgezondheidenzorg.info/onderwerp/sterfte/cijfers-context/huidige-situatie#node-relatieve-sterfte-naar-leeftijd-en-geslacht
Los efectos secundarios de la vacuna de Pfizer/BioNTech:
No debería sorprender que una vacuna eficaz tenga más efectos secundarios (leves). El sistema inmunitario se activa, lo que puede compararse mejor con una orquesta sinfónica que empieza a tocar. Se activan muchas células diferentes, células T y células B, pero también muchas otras células y todas estas células producen sustancias de señalización llamadas citoquinas que conducen a síntomas similares a los de la gripe que también pueden ocurrir con una infección por el propio virus.
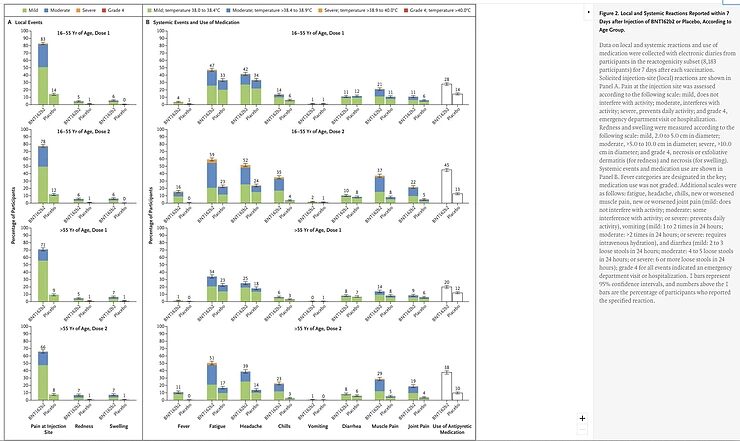
Estos efectos secundarios pueden dividirse en locales y sistémicos. Especialmente, el efecto secundario local del dolor fue mucho más frecuente en el grupo que se vacunó, unas ocho veces más en comparación con el grupo que recibió el placebo. Los efectos secundarios sistémicos de dolor de cabeza y fatiga fueron dos veces más frecuentes en el grupo vacunado.
Aunque se trata de efectos secundarios relativamente leves y transitorios, estas diferencias en el grado de efectos secundarios ponen en peligro la imparcialidad del estudio. Es concebible, e incluso posible, que las personas que experimentaron muchos efectos secundarios por la inyección asuman que recibieron la vacuna y, por tanto, sean menos propensas a atribuir al COVID-19 cualquier dolencia inespecífica como el dolor de cabeza, el dolor muscular y la tos y, por tanto, no informen de ellos. Esto es aún más difícil porque no se ha descrito qué molestias en uno u otro grupo llevaron a sospechar que se trataba del COVID-19 y cuán frecuentes y graves eran estas molestias.
Si resulta que las personas que tenían COVID-19 y recibieron la vacuna informaron en promedio muchas más quejas y más graves que las personas del grupo de placebo a las que se les diagnosticó COVID-19, esto sería una indicación de que el grupo vacunado no interpretó las quejas más leves como una expresión de COVID-19 y, por lo tanto, no las informó. Además, si bien los investigadores no sabían quiénes recibieron la vacuna y quiénes no, sí conocían registro de los efectos secundarios, y esto puede haber influido en la decisión de hacer o no la prueba a alguien. También quiero mencionar que las personas que administraron las vacunas o el placebo sí estaban informadas. La pregunta es, por tanto, hasta qué punto interactuaban con los investigadores.
En cuanto a los efectos secundarios en sí, es totalmente justificable que la gente tenga molestias tan leves por una vacuna si es para prevenir una infección grave y potencialmente mortal. Y cabe preguntarse si este es el caso. La mortalidad entre las 21.728 personas que recibieron el placebo es exactamente... ¡cero!
Los resultados del estudio:
Estos son los resultados del efecto de la vacuna contra el virus del SARS-CoV-2 en la medida de resultado primaria descrita anteriormente. Efectivamente, la probabilidad de tener dolencias leves e inespecíficas en el grupo vacunado es un 95% menor. Sin embargo, en mi opinión esta es una medida de resultado irrelevante, de valor cero. La medida en que una vacuna es capaz de prevenir dolencias relativamente leves -como también se observan en una gripe, un resfriado o una gastroenteritis leves- no tiene, en mi opinión, ningún valor, mientras la vacuna se apruebe y se autorice sobre la base de estos datos. En definitiva, se trata de 169 personas con estas molestias en el grupo de placebo y 9 personas en el grupo vacunado.
"La COVID-19 confirmada se definió según los criterios de la Food and Drug Administration (FDA) como la presencia de al menos uno de los siguientes síntomas: fiebre, tos nueva o aumentada, dificultad respiratoria nueva o aumentada, escalofríos, dolor muscular nuevo o aumentado, pérdida nueva del gusto o del olfato, dolor de garganta, diarrea o vómitos, combinados con una muestra respiratoria [es decir, un resultado positivo de la RT-PCR] obtenida durante el periodo sintomático o en los 4 días anteriores o posteriores"¡Por favor, tome nota! Permítame decirlo de nuevo: sólo una de estas quejas no específicas, como se mencionó anteriormente, fue suficiente para dar el diagnóstico clínico de COVID-19.
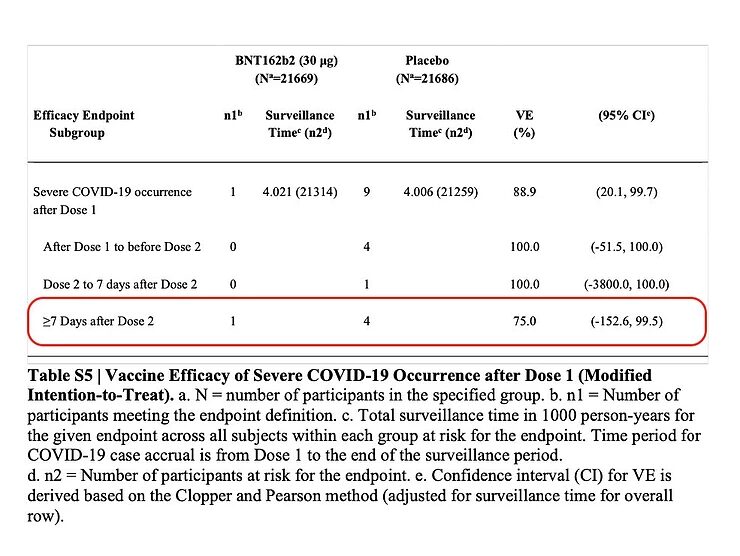
Por supuesto, me gustaría saber hasta qué punto la vacuna es capaz de prevenir la "COVID-19 grave". Por desgracia, eso no se menciona en el artículo y tengo que buscarlo en el suplemento del artículo. Si se mira a los 7 días de la 2ª dosis de la vacuna, parece que hubo cuatro casos de COVID-19 grave en el grupo placebo y uno en el grupo vacunado.
Ahora bien, existe un número llamado "Número necesario para vacunar", y aunque se entiende que se trata de conceptos diferentes en la literatura, es ilustrativo mostrar aquí cuántas personas deben ser vacunadas para prevenir un caso de "COVID-19 grave". Es decir, 19.965/(4-1) = 6555 personas. Por supuesto, este Número Necesario para Vacunar disminuirá a medida que más personas enfermen, y lo que es más, estas cifras no son más que ruido estadístico.
Sin embargo, un punto importante es que no sabemos cuántas personas del grupo de placebo se infectaron realmente con el virus del SARS-CoV-2. Lo que podría haberse llevado a cabo fácilmente como estudio paralelo es el mapeo de cuántas personas del grupo placebo desarrollaron anticuerpos para estimar cuántas personas tuvieron realmente una infección con el virus del SARS-CoV-2 en el periodo del estudio, para determinar qué proporción de personas estaban todavía "en riesgo" de contraer la infección. Sin embargo, esto no se ha hecho y, en mi opinión, es una de las principales deficiencias de este estudio. Es fácil de entender desde la perspectiva del productor, que quiere vender tantas vacunas como sea posible. No le interesa demostrar que una gran proporción de personas ya no necesitan su vacuna porque ya se han infectado con el virus del SARS-CoV-2.
Además, me parece muy llamativo que los autores se atrevan a afirmar, basándose en estas cifras, que la probabilidad "teórica" de "aumento de la enfermedad mediada por la vacuna" es insignificante. Con una frecuencia tan baja de la enfermedad, esta es una conclusión muy prematura, ya que se trata de un fenómeno raro.
La seguridad de la vacuna:
¿Qué escriben los autores sobre la seguridad de la vacuna? Dicen que hay un 83% de probabilidades de descubrir un efecto secundario relevante si el efecto secundario en cuestión ocurre con más frecuencia que en 1 de cada 10.000 vacunados (0,01%). Esto también significa automáticamente que hay un 17% de probabilidades de que ese efecto secundario adverso no se detecte con esa frecuencia de aparición. Los efectos secundarios más raros, o que sólo se producen en una fase posterior, no pueden, por supuesto, encontrarse con esta investigación.
Comentario: Vea también: Desastre: 20% de los sujetos de prueba humanos de Moderna tuvieron lesiones severas de la vacuna contra el coronavirus de Gates-Fauci (en inglés)
Lo que me parece especialmente preocupante, y no entiendo por qué los editores del NEJM lo aprobaron, es que los autores del artículo argumentan que sería (éticamente) injustificado evaluar la seguridad y eficacia de la vacuna en el contexto de la continuación del estudio a doble ciego. Esto implica que pretendían vacunar también al grupo placebo. Hacer esto erradicará definitivamente la posibilidad de atribuir cualquier efecto secundario grave a la vacuna con certeza. Esto conviene directamente al interés del productor de la vacuna en el contexto de cualquier responsabilidad, incluso si esta responsabilidad ha sido depositada ante las autoridades nacionales.
Comentario: Vea también: No se puede demandar a Pfizer o Moderna si se tienen efectos secundarios severos de la vacuna Covid. Lo más probable es que el gobierno tampoco compense por daños. (en inglés)
Además, me pregunto por qué habría que romper el cegamiento y por qué no sería ético continuar el estudio en su configuración original, ya que la tasa de mortalidad por infección (IFR) de los participantes en el estudio es muy baja, y la pregunta sigue siendo si la vacuna les beneficiará. Esa es precisamente la pregunta de investigación del estudio a largo plazo.
Lo que me pregunto por encima de todo es por qué Pfizer/BioNTech piensa aparentemente que es ético vacunar a niños menores de 12 años en un contexto de investigación contra el virus del SARS-CoV-2, una infección que no hace, o apenas hace, que los niños enfermen. Además, la probabilidad de que puedan morir por ella es prácticamente nula. La probabilidad de que los niños mueran a causa de una infección por el virus SARS-CoV-2 es, lo más probable, menor que la probabilidad de morir a causa de una infección por el virus de la gripe.
Por lo tanto, estoy francamente desconcertado de que con una tasa de mortalidad por infección tan extremadamente baja en estos grupos de edad, Pfizer/BioNTech haya recibido aparentemente el permiso de las distintas autoridades para vacunar a los niños en un contexto de investigación con una vacuna experimental que, como se ha mencionado, no se ha utilizado antes.
Los autores se exceden de nuevo en la discusión, y me temo que esta frase viene directamente del departamento de relaciones públicas de Pfizer/BioNTech, afirmando lo siguiente: "La rigurosa demostración de seguridad y eficacia menos de 11 meses después... "
Sin embargo, todavía no se ha demostrado nada "riguroso"; los resultados no son más que una indicación, los resultados finales tardarán años en llegar.
¿Cuál es la conclusión final?
Estas son las preguntas pertinentes a las que debería responder un estudio adecuado sobre la eficacia y la seguridad de una vacuna:
- ¿Cuál es el efecto de la vacuna de Pfizer/BioNTech sobre el número de ingresos hospitalarios, el número de ingresos en cuidados intensivos y la mortalidad?
- ¿Cuál es la eficacia a largo plazo de la vacuna, en este caso un periodo superior a dos meses?
- ¿Cuál es la seguridad a largo plazo de la vacuna, en este caso un periodo superior a dos meses?
- ¿Qué sabemos de los efectos secundarios más raros pero posiblemente graves, como los trastornos autoinmunes, que también pueden producirse a largo plazo y para los que esta investigación no tenía la duración y la potencia necesarias?
- ¿Es capaz la vacuna de romper la cadena de transmisión, es decir, impedir la transmisión del virus de una persona a otra?
Lo que se está poniendo en marcha ahora es un experimento masivo de vacunas como no se ha visto antes, con sólo datos mínimos sobre la seguridad y la eficacia de la vacuna utilizada. Es muy posible que dentro de unos años se llegue a la conclusión de que esta nueva técnica de ARNm ha dado lugar a una vacuna segura y eficaz, pero esa conclusión ahora es extremadamente prematura y muy arriesgada. No sería la primera vez que se producen accidentes importantes como consecuencia de la precipitación y la imprudencia, como se señaló recientemente con razón en un editorial de JAMA. https://jamanetwork.com/journals/jama/fullarticle/2766651
Además, el hecho de que la vacuna Pandemrix contra la gripe porcina, que fue promocionada por Ab Osterhaus (entre otros) como un "virus asesino", al examinarla más detenidamente se descubrió que era uno de los virus de la gripe más benignos de todos los tiempos, debería advertirnos contra las grandes prisas y los alarmantes descuidos. Pero aparentemente los políticos, los administradores, muchos académicos -y sí, también muchos médicos- están sordos y ciegos a las lecciones que la historia deberían haberles enseñado.
Por último, me gustaría sugerir que las damas y caballeros altamente educados (eruditos legales, éticos y filósofos, gente como Roland Pierik, Marcel Verweij, Gert van Dijk, Brigit Toebes y Martin Buijsen) primero se sumerjan a fondo en el asunto antes de intentar inyectar la vacuna a la fuerza en el brazo del pueblo holandés, como verdaderos fascistas de las vacunas. La propaganda acrítica de una vacuna que todavía no ha demostrado ni remotamente su valor, eficacia y seguridad es extremadamente perjudicial para el uso de otras vacunas que han demostrado su seguridad y eficacia y, de hecho, conviene a las mismas personas que rechazan categóricamente cualquier forma de vacunación.
Jan B. Hommel es un neurólogo holandés. Su blog se puede encontrar aquí.













Comentarios del Lector
a nuestro Boletín